phمتر
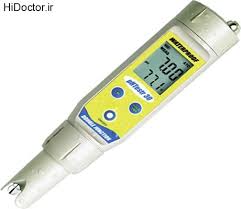
واژه PH (پ هاش) برای نشان دادن درجه اسیدی یا قلیایی بودن یک محلول به کار میرود. درواقع پ هاش لگاریتم منفی غلظت یون هیدروژن (هیدرونیوم) در محلول آب است؛
یعنی: ph=-log10 H+
H+ غلظت یون هیدروژن را بیان میکند.
بااینکه ممکن است یونهای مختلفی در محلول شکل بگیرند، ولی آنهایی که تعیین میکنند محلول اسیدی یا قلیائی است، به ترتیب یون هیدروژن (H+) و یون هیدروکسیل (OH-) هستند. زمانی که تعداد یونهای هیدروژن از تعداد یونهای هیدروکسیل در محلول بیشتر باشد، محلول اسیدی است. وقتیکه تعداد این دو یون برابر باشد، محلول خنثی است. زمانی که تعداد یونهای هیدروژن از تعداد یونهای هیدروکسیل در محلول کمتر باشد، محلول قلیایی (بازی) است.
میزان تشکیل یون در محلول، برای اسیدها و قلیاها متفاوت است. آن دستهای که تقریباً بهطور کامل یونیزه میشوند، اسید یا باز قوی هستند. هیدرو کلرید اسید و سدیم هیدروکسیل مثالهایی برای این دستهاند. بقیه اسیدها و بازهای به مقدار کمی یونیزه میشوند و اسید یا باز ضعیف هستند. استیک اسید و آمونیوم هیدروکسیل نمونههایی برای این گروه میباشند. میتوان اسیدها و بازها را بنا بر تعداد یون هیدروژنی که در هر مولکول میتوانند از دست دهند، دستهبندی کرد. اگر اسیدی در هر مولکولش فقط یک یون هیدروژن آزاد کند، به آن اسید تکظرفیتی میگویند.
حتی آب خالص نیز به مقدار خیلی کم به یون هیدروژن و هیدروکسیل تبدیل میشود. در دمای 25 درجه سانتیگراد، آب خالص همواره دارای 0.0000001 یا 1×10-7 گرم اکی والان در لیتر یون هیدروژن دارد و چون آب خالص خنثی است به همین میزان یون هیدروکسیل نیز دارد.
حاصلضرب این دو غلظت برابر با مقدار ثابت 1.0×10-7 در 25 درجه سانتیگراد است.
اگر غلظت یون هیدروژن یک محلول 1.0×10-4 گرم اکی والان در لیتر باشد، غلظت یون هیدروکسیل در این محلول برابر 1.0×10-10 گرم اکی والان در لیتر خواهد بود. چون در این مورد غلظت یون هیدروژن بیشتر از غلظت یون هیدروکسیل است، محلول اسیدی است.
برای سادهتر بیان کردن غلظت یون هیدروژن، بهجای بیان آن با اعداد اعشاری و توانهای منفی، مفهوم PH تعریفشده است. بیان ریاضی این مفهوم، برابر با منفی لگاریتم غلظت یون هیدروژن در مبنای 10 است. محلولی با غلظت یون هیدروژن برابر 1.0×10-7 گرم اکی والان در لیتر PH برابر 7 دارد.
ازآنجاییکه در محلولهای اسیدی غلظت یون هیدروژن بیشتر از 1.0×10-7 گرم اکی والان در لیتر است، مقدار PH آنها کمتر از 7 است. بلعکس محلولهای قلیایی PH بالاتر از 7 دارند.
مهم است که به یاد داشته باشید، تغییر یک واحد در PH برابر با 10 برابر تغییر در اسیدیته یا قلیایی بودن محلول است؛ بنابراین یک محلول با PH=4 در مقایسه با محلولی با PH=5، 10 برابر اسیدیتر است، محلولی با PH=3 در برابر محلولی با PH=5، 100 برابر اسیدیتر است و محلولی با PH=2 در برابر محلولی با PH=5، 1000 برابر اسیدیتر است. محدوده پذیرفتهشده برای تغییرات PH از 0 تا 14 است.
برای اندازهگیری آن از دستگاه پ هاش متر استفاده میکنند

نظرات
نظر بدهید